Content
Dit onderwerp is toegespitst op de compliantie van het respiratoire systeem met name tijdens respiratoire ondersteuning.
Equation of Motion
De equation of motion, of de bewegingsvergelijking, beschrijft de drukverandering op het niveau van de luchtwegopening tijdens mechanische ventilatie (positieve druk beademing). Zowel tijdens de inspiratie als expiratie:
- P: druk bij de luchtwegopening (mond of endotracheale tube)
- V: longvolume
- C: Compliantie van het respiratoire systeem
- Q: flow
- R: luchtwegweerstand
- Pmus: druk gegenereerd door de ademhalingsspieren
De beademingsdrukken zijn dus afhankelijk van het teugvolume, de compliantie, de weerstand, de inspiratoire flow en de bijdrage van de ademhalingsspieren van de patiënt zelf (dit laatste indien er geen sprake is van volledig gecontroleerde beademing).
Definitie compliantie
Er zijn meerdere definities beschreven voor compliantie van het respiratoire systeem. Er moet met name een verschil gemaakt worden tussen statische compliantie en dynamische compliantie1.
- Statische compliantie: de verandering in longvolume per verandering in druk bij afwezigheid van flow. Deze is samengesteld uit:
- Thoraxwand compliantie
- Longweefsel compliantie
- Dynamische compliantie: de verandering in longvolume per eenheid verandering in druk in aanwezigheid van stroming. Deze is samengesteld uit:
- Thoraxwand compliantie
- Longweefsel compliantie
- Luchtwegweerstand
Om het simpel te houden baseer ik mijn klinische redenaties met betrekking tot compliantie op de statische compliantie:
De luchtwegweerstand is een aparte entiteit en bespreek ik als een apart onderwerp.
De componenten van compliantie
De druk-volume relatie is afhankelijk van verschillende factoren, grofweg in te delen in twee groepen: thoraxwand (200 ml/cmH2O) en de long zelf (200 ml/cmH2O). Een normaalwaarde voor de totale respiratoire compliantie is 100 ml/cm H2O
Met de transpulmonale druk (gemeten met een oesophagusballon) kan de longcompliantie worden gescheiden van de thoraxwandcompliantie.
Hieronder de factoren die invloed hebben op de compliantie:
Longcompliantie
Toegenomen longcompliantie
- Longsurfactant
- Longvolume, de compliantie is het hoogst rondom de FRC
- PEEP
- Positie (liggend, staand)
- Emfyseem
Afname longcompliantie
- Verlies van surfactant (bijv. ARDS)
- Verminderde long elasticiteit
- Fibrose
- Oedeem
- Verminderde functioneel longvolume
- Pneumonectomie of lobectomie
- Pneumonie
- Atelectase
- Kleine lichaamsbouw
- Alveolaire collaps
- Alveolaire overdistentie
Thoraxwandcompliantie
Toename thoraxwandcompliantie
- Ehler-Danlos-syndroom en andere bindweefselziekten geassocieerd met verhoogde elasticiteit van het bindweefsel
- Ribresectie
- Cachexie
- Ribfracturen
- Open thorax (bijv. Clamshell)
Afname thoraxwandcompliantie
- Structurele afwijkingen
- Kyfose / scoliose
- Pectus excavatum
- Perifere brandwonden
- Chirurgische ribfixatie
- Functionele afwijkingen
- Spierspasmen, bijv. insult of tetanus
- Extrathoracale invloeden op de thorax / diafragmatische excursie
- Obesitas
- Abdominaal compartimentsyndroom
- Buikligging
- Overig: pneumothorax
Druk-volume curve
De compliantie is de relatie tussen druk en volume. Deze relatie veranderd continu gedurende een ademteug. Hieronder een hypothetische druk-volume curve / loop waarbij de maximale druk hoog is.
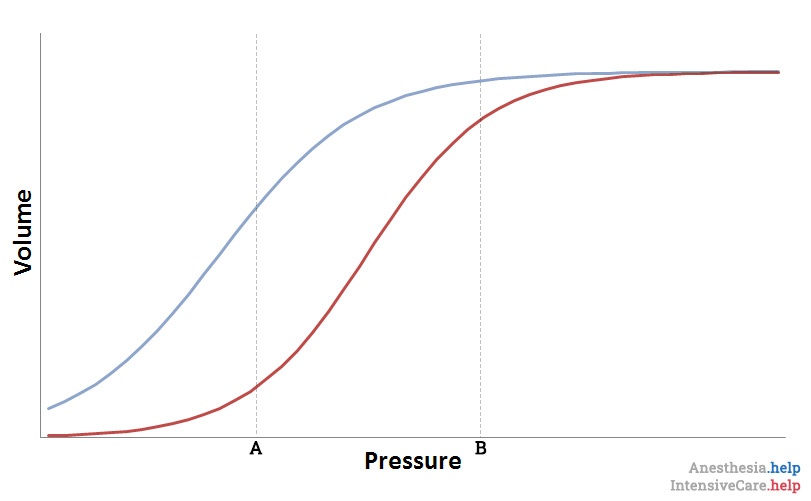
Belangrijke aspecten van deze curve bespreek ik hieronder:
Optimale compliantie
Dit is het gedeelte van de curve waar de inspiratoire (rode) lijn het steilst is (tussen A en B). Hier is de druk zodanig dat alveoli allemaal open zijn en geleidelijk uitzetten naarmate druk toeneemt.
Onderste inflectie punt
Het onderste inflectie punt (punt A in de grafiek) representeert de openingsdruk van de alveoli, dit is een reflectie van de alveolaire recruitment. Het kost meer druk een gecollabeerde alveoli te openen dan een reeds geopende alveoli te vergroten. Dit is onder andere te verklaren met de wet van Laplace. Tevens heeft surfactant hier ook invloed op.
PEEP titratie
Bij ARDS is gedacht dat dit lage inflectie punt de PEEP zou moeten bepalen volgens het ‘open lung concept’. Gezien het feit dat het constant collaberen en opnieuw openen van alveoli ‘ventilator induced lung injury’ veroorzaakt. Fysiologisch een logisch concept. Het concept waarbij PEEP wordt getitreerd d.m.v. het onderste inflexie punt is echter in twijfel getrokken omdat deze benadering beperkingen heeft: het onderste inflexiepunt is oa. slecht bepaalbaar 2 en er is lastig bewijs te vinden dat PEEP titratie op de compliantie de mortaliteit, beademingsdagen en IC-opname duur verminderd. Hieronder een korte samenvatting van trials met verschillende PEEP-titreer strategieën bij ARDS, vaak vergeleken met de ARDSnet PEEP tabellen (die gebaseerd zijn op met name expert opinion) 3:
- Armato, 2015, NEJM (meta-analyse door middel van een multilevel mediation analysis van 9 RCT’s): Beademen met een lage driving pressure, oftewel in het gedeelte van de curve met de optimale compliantie (waarbij de PEEP dus boven het onderste inflexie punt moet liggen) is geassocieerd met minder mortaliteit 4.
- ART-trail, 2017, JAMA (RCT): een strategie met recruitment (staircase recruitment maneuver) en getitreerde PEEP op beste compliantie vergeleken met een lage PEEP verhoogde de 28-dagen mortaliteit 5. Het is mij echter onduidelijk of de PEEP-titratie op de beste compliantie of juist de routinematige agressieve alveolaire recruitment manoeuvres hebben bijgedragen aan het negatief effect op de resultaten. Een mogelijke reden voor de hogere mortaliteit betreft de mechanische power geleverd aan de long tijdens recruitment, ook routinematig bij niet-responders. Bij de ‘mild’ ARDS-longen was mechanische power driemaal groter dan bij de ‘severe’ ARDS-longen 6. Ruim 59% van de studiepopulatie had ‘moderate’ ARDS en bij de subgroup analyse van de ART-trail was de mortaliteit ook niet verschillend in de ‘severe’ ARDS groep.
- PHARLAP, 2019, AJRCCM (RCT): Maximale routinematige recruitment (staircase recruitment maneuver) en PEEP getitreerd op hypoxie verminderd niet de duur van ventilatievrije dagen of mortaliteit. Er was associatie met verhoogde cardiovasculaire bijwerkingen, maar minder noodzaak tot gebruik van rescue therapie voor hypoxie 7.
- Briel, 2010, JAMA (meta-analyse): Een hoog versus laag niveau van PEEP was niet geassocieerd met een verbeterde ziekenhuisoverleving. Echter waren hogere PEEP niveaus wel geassocieerd met verbeterde overleving bij de subgroep van patiënten met ernstige ARDS 8.
- Mercat, Express Study Group, 2008, JAMA (RCT): PEEP titratie gericht op toenemende alveolaire recruitment en beperking van hyperinflatie had geen significante invloed op de afname van mortaliteit. Het verbeterde echter de longfunctie, verkortte de duur van mechanische ventilatie en de duur van orgaanfalen 9.
- Brower, 2004, NEJM (RCT): Bij mechanische ventilatie bij ARDS met een streefvolume van 6 ml/kg IBW en een eindinspiratoire plateau druklimiet van 30 cmH2O zijn de klinische resultaten vergelijkbaar met lage of hoge PEEP-niveaus 10.
Bij niet zieke longen (tijdens algehele anesthesie voor abdominale chirurgie) is aangetoond dat de getitreerde PEEP op basis van electrical impedance tomography (tegengaan van collaps en hyperdistensie) peroperatief leidt tot een verminderde driving pressure en verbeterde oxygenatie en postoperatief voor een afname van de incidentie van atelectase 11. Dit zegt echter niets over klinische uitkomsten als pulmonale complicaties. Verder viel op dat het interindividuele verschil in de beste PEEP voor optimale longcompliantie bij gezonde longen groot was, wellicht bepaald door met name de thoraxwandcompliantie.
Bovenste inflectie punt
Het bovenste inflectie punt (punt B in de grafiek) zou overrek van de long representeren. Echter bij compliantieproblematiek zoals bij ARDS is heterogeniciteit het probleem. Dit betekend dat op dit punt al significante delen van de long overdistenderen waarbij andere longdelen mogelijk nog zijn gecollabeerd. Daardoor vlakt dit punt af, is het moeilijker te bepalen en is de klinische waarde minder aanwezig.
Er zijn ook berichten in de literatuur dat het bovenste infectie punt zich in de expiratoire curve zou moeten bevinden 12.
Alveolaire overdistentie
In de regio boven het bovenste inflectie punt leidt een toename van druk niet tot veel meer volume. De long is overrekt. Dit is dus een gebied op de curve waar de druk niet veel zal bijdragen aan het volume en aan de ventilatie.
Hysterese
Opvallend bij de druk-volume loop is het verschil in druk-volume relatie tussen inspiratie (rood) en expiratie (blauw). Dit wordt hysterese genoemd. De longvolume bij een bepaalde druk tijdens inademing is kleiner dan het longvolume bij een bepaalde druk tijdens uitademing. De oorzaak hiervan is:
- Recruitment en collaps van alveoli: openen van alveoli kost meer druk
- Het effect van alveolaire oppervlakte spanning en wandspanning (wet van Laplace)
- Stress relaxatie: energieverlies in het longweefsel door rek
- Gasabsorptie tijdens de meting 13
Compliantie en mechanische beademing
De totale compliantie (zowel long als thoraxwand) tijdens positieve druk beademing is te meten in de drukcurve bij volume gecontroleerde beademing door middel van ‘inspiratory pause’.

Inspiratory pause
Zoals aan het begin van dit artikel beschreven wordt volgens de equation of motion bij volume gecontroleerde beademing de druk gegenereerd door een constante flow, de longcompliantie, de luchtwegweerstand en het teugvolume. Door de inspiratie te beëindigen en de adem in te houden, wordt de bijdrage van de weerstand geëlimineerd en blijft alleen de druk over die afhankelijk is van de longcompliantie en het teugvolume. Zie de bovenstaande schematische weergave van de drukcurve bij een volume gestuurde ademteug.
- Het verschil tussen PEEP en plateau pressure is toe te schrijven aan de compliantie van de long en de thoraxwand bij elkaar.
- Het is de druk die nodig is om het volume in de long (indien er geen flow meer is) te genereren (de eenheid is: cmH2O/L).
- Om alleen de longcompliantie te meten is het noodzakelijk de druk in de intra-pleurale ruimte te weten. Dan kan de transpulmonale druk worden berekend waarmee op zijn beurt de longcompliantie bepaald kan worden. De intra-pleurale druk is niet meetbaar. Een surrogaat is de oesofagusdruk.
- De meest nauwkeurige manier om dit te meten is bij een verslapte patiënt. De meeste ventilatoren kunnen dit automatisch.
Interpretatie ventilator curves
Tijdens mechanische beademing geven de beademingscurves veel informatie over de mate van compliantie en kunnen bijvoorbeeld bij een acute respiratoire insufficiëntie als diagnosticum fungeren waarmee de differentiaal diagnose dan gezocht kan worden in de componenten van compliantie.
Volume gestuurd / Volume control
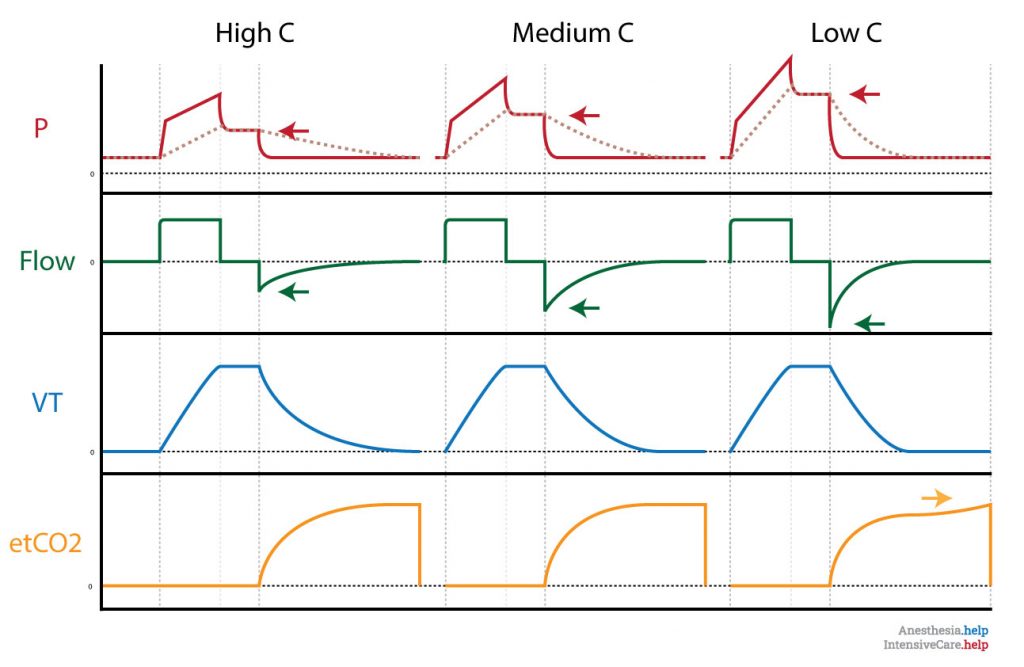
Bij een volume gecontroleerde modus leidt een afname van de compliantie tot een toename van de plateaudruk. In tegenstelling tot bij een verhoogde luchtwegweerstand is er geen stijging van de drukgradiënt tussen piekdruk en plateaudruk.
Tijdens de uitademing genereert de toename van de drukgradiënt tussen de alveolaire druk (donker rood gestippelde lijn) en de ademwegdruk een flowverhoging (groene pijlen) en verkort daarmee de tijd die nodig is voor de uitademing. Dit beïnvloed de tijdconstante van de expiratie.
Bij een lage compliantie kan er een terminale ‘upswing’ of ‘pigtail’ ontstaan in het capnogram (etCO2). Zie de gele pijl. Het treedt op wanneer een slecht compliante long (of slecht compliante thoraxwand bij obesitas of de zwangerschap) collabeert en de kleine bronchiën afsluit waardoor de laatste milliliters CO2 uit de alveoli geperst wordt.
Druk gestuurd / Pressure Control
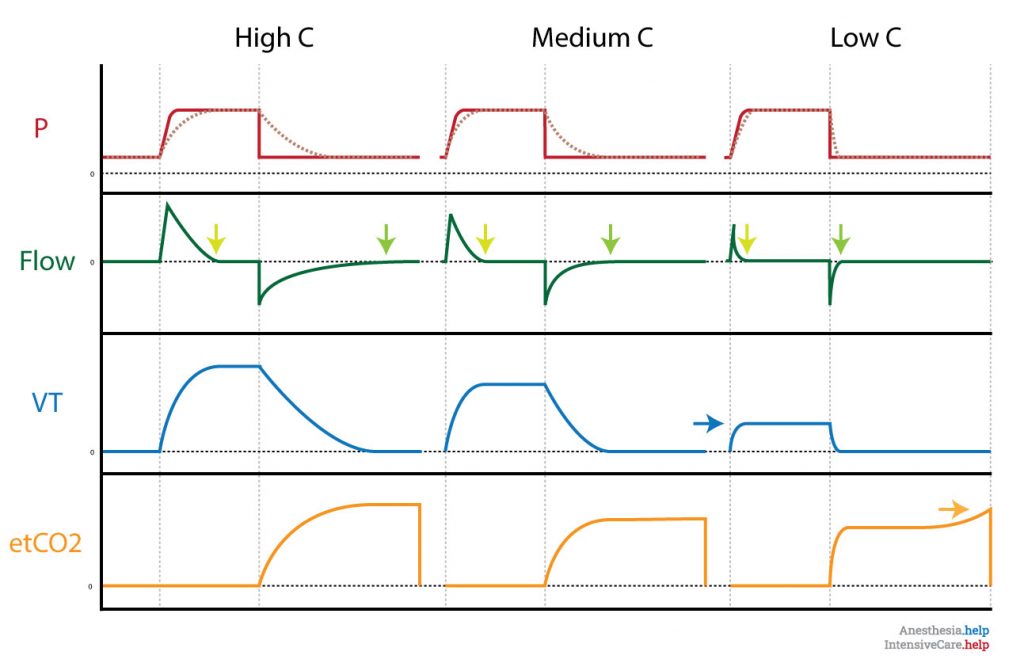
Als een drukgestuurde modus wordt toegepast zorgt een afname van de compliantie voor het sneller bereiken van de alveolaire druk (donker rood gestippelde lijn) tijdens inspiratie, de flow neemt dus sneller af, de inspiratoire pauze wordt verlengd en de het teugvolume neemt af.
De expiratie vind hetzelfde (namelijk passief) plaats als bij een volume gecontroleerde beademing. Echter blijft de maximale expiratoire flow zo goed als gelijk maar is de expiratie met name kort (zie de groene pijlen). Dit omdat de gradient gelijk blijft (deze is ingesteld) maar het teugvolume afneemt (blauwe pijl).
Referenties
- 1.Harris R. Pressure-volume curves of the respiratory system. Respir Care. 2005;50(1):78-98; discussion 98-9. https://www.ncbi.nlm.nih.gov/pubmed/15636647.
- 2.SCOTT HARRIS R, HESS DR, VENEGAS JG. An Objective Analysis of the Pressure-Volume Curve in the Acute Respiratory Distress Syndrome. Am J Respir Crit Care Med. February 2000:432-439. doi:10.1164/ajrccm.161.2.9901061
- 3.Ventilation with Lower Tidal Volumes as Compared with Traditional Tidal Volumes for Acute Lung Injury and the Acute Respiratory Distress Syndrome. N Engl J Med. May 2000:1301-1308. doi:10.1056/nejm200005043421801
- 4.Amato MBP, Meade MO, Slutsky AS, et al. Driving Pressure and Survival in the Acute Respiratory Distress Syndrome. N Engl J Med. February 2015:747-755. doi:10.1056/nejmsa1410639
- 5.Cavalcanti AB, Suzumura ÉA, et al. Effect of Lung Recruitment and Titrated Positive End-Expiratory Pressure (PEEP) vs Low PEEP on Mortality in Patients With Acute Respiratory Distress Syndrome. JAMA. October 2017:1335. doi:10.1001/jama.2017.14171
- 6.Cipulli F, Vasques F, Duscio E, Romitti F, Quintel M, Gattinoni L. Atelectrauma or volutrauma: the dilemma. J Thorac Dis. March 2018:1258-1264. doi:10.21037/jtd.2018.02.71
- 7.Hodgson CL, Cooper DJ, Arabi Y, et al. Maximal Recruitment Open Lung Ventilation in Acute Respiratory Distress Syndrome (PHARLAP). A Phase II, Multicenter Randomized Controlled Clinical Trial. Am J Respir Crit Care Med. December 2019:1363-1372. doi:10.1164/rccm.201901-0109oc
- 8.Briel M, Meade M, Mercat A, et al. Higher vs Lower Positive End-Expiratory Pressure in Patients With Acute Lung Injury and Acute Respiratory Distress Syndrome. JAMA. March 2010:865. doi:10.1001/jama.2010.218
- 9.Mercat A, Richard J-CM, Vielle B, et al. Positive End-Expiratory Pressure Setting in Adults With Acute Lung Injury and Acute Respiratory Distress Syndrome. JAMA. February 2008:646. doi:10.1001/jama.299.6.646
- 10.Higher versus Lower Positive End-Expiratory Pressures in Patients with the Acute Respiratory Distress Syndrome. N Engl J Med. July 2004:327-336. doi:10.1056/nejmoa032193
- 11.Pereira SM, Tucci MR, Morais CCA, et al. Individual Positive End-expiratory Pressure Settings Optimize Intraoperative Mechanical Ventilation and Reduce Postoperative Atelectasis. Anesthesiology. December 2018:1070-1081. doi:10.1097/aln.0000000000002435
- 12.Albaiceta GM, Taboada F, Parra D, et al. Tomographic Study of the Inflection Points of the Pressure–Volume Curve in Acute Lung Injury. Am J Respir Crit Care Med. November 2004:1066-1072. doi:10.1164/rccm.200312-1644oc
- 13.Lung histeresis: a morphological view. Histology and Histopathology. January 2004:159-166. doi:10.14670/HH-19.159